Отзывы после удаления рака простаты, Лечение рака простаты в Израиле
Сколько стоит лечение рака простаты в Израиле Стоимость диагностических и лечебных мер в больницах страны регулируется Министерством Здравоохранения Израиля. Рак предстательной железы РПЖ имеет различные варианты лечения и высокие показатели продолжительности жизни после их применения. Вы записываетесь к врачу. Химиотерапию в клинике «Медскан» можно проходить в амбулаторных условиях или в стационаре.
Брюшную полость заполняют углекислым газом, чтобы увеличить объем рабочего пространства для хирурга. Сидя за консолью, врач управляет несколькими многошарнирными роботизированными руками. Они в точности повторяют движение рук хирурга, но при этом могут поворачиваться на градусов и действуют с непревзойденной точностью.
Камера эндоскопа передает на экран монитора многократно увеличенное трехмерное изображение операционного поля с высоким разрешением.
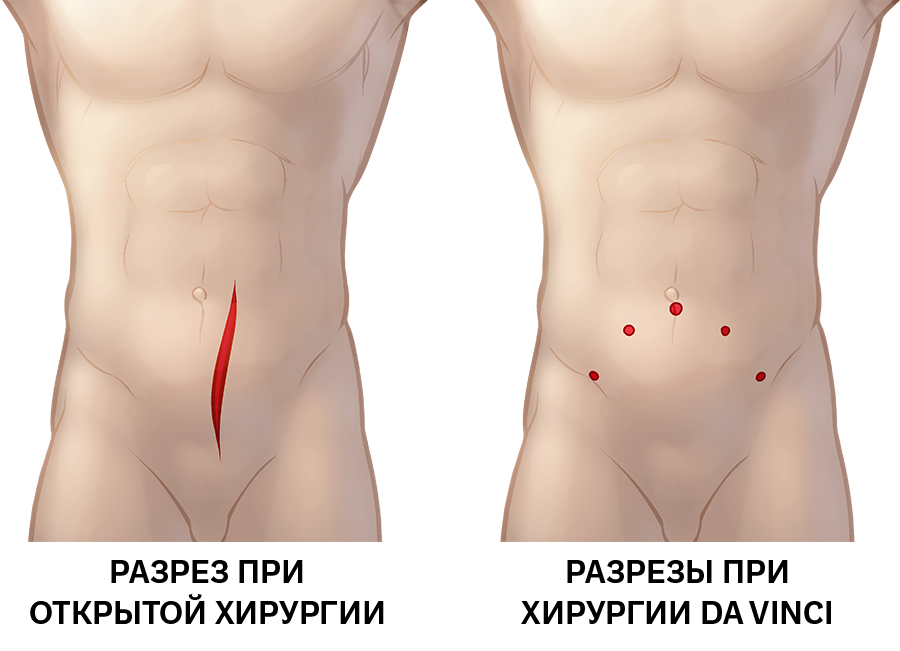
Хирург отделяет предстательную железу от мочевого пузыря и уретры, сохраняя окружающие тонкие нервные сплетения. Это позволяет сохранить нормальную мочеиспускательную и эректильную функцию после операции. Please leave this field empty. Укажите свое имя. Введите номер телефона. Опишите Вашу ситуацию. Операция проводится через один небольшой разрез.
Благодаря минимальной инвазивности она больше похожа на амбулаторную процедуру, чем на полноценное хирургическое вмешательство. Однопортовая простатэктомия связана с меньшим риском осложнений и боли при восстановлении. После нее не остается заметного рубца, а пациенты могут вернуться домой в тот же день. Для сравнения установки Да Винчи предыдущих поколений, которые до сих пор используются для проведения простатэктомии, оснащены четырьмя роботическими руками.
Соответственно для операции необходимо сделать 5 небольших разрезов в брюшной стенке. Ключевая особенность однопортовой хирургии состоит в том, что эта техника позволяет хирургу манипулировать в небольшой полости, называемой экстраперитонеальным пространством.
При использовании предыдущих моделей Да Винчи хирург манипулирует во всей брюшной полости, поэтому всегда сохраняется риск повреждения кишечника. При однопортовой хирургии этот риск сводится практически к нулю. Ограничение операционного поля экстраперитонеальным пространством значительно снижает травматичность операции. Поэтому пациенты могут вернуться домой всего через несколько часов после хирургического вмешательства.
Радикальная простатэктомия — это очень сложная операция, которая требует высокого уровня технической точности. Простата окружена нервами и структурами, которые критически важны для сохранения нормального мочеиспускания и половой функции. Возможные осложнения простатэктомии могут значительно снижать качество жизни пациентов, поэтому многие из них ищут способы, как их избежать.
К счастью в последние годы в области хирургии простаты произошли существенные положительные изменения. Применение минимально инвазивных техник, высокотехнологичных роботизированных установок, а также современных методов предоперационной визуализации позволили свести риск осложнений простатэктомии к минимуму. Кроме этого, исследования показали, что у хирургов, регулярно выполняющих радикальное удаление простаты, количество осложнений меньше, чем у тех, кто реже проводит эти операции.
Поэтому при выборе клиники следует отдавать предпочтение крупным многопрофильным центрам, которые располагают отделениями, специализирующимися на хирургическом лечении рака простаты. Из наиболее востребованных и популярных медицинских центров за рубежом можно выделить:. Стоимость простатэктомии зависит от метода проведения операции, ценовой политики клиники, а также объема и сложности хирургического вмешательства.
Чтобы узнать больше о хирургическом лечении рака простаты, позвоните по одному из телефонов, указанных на сайте или заполните онлайн-форму.

Врач-координатор свяжется с вами в самые краткие сроки. Он поможет подобрать клинику и врача для проведения операции, учитывая ваши персональные потребности и пожелания. Несмотря на то, что простатэктомия остается золотым стандартом хирургического лечения рака предстательной железы, как и любая операция она связана с риском побочных эффектов.
В некоторых случаях. Однако в случае агрессивного течения рака, без операции не обойтись. Второе мнение — это услуга, которая позволяет пациента убедиться в том, что ему поставили правильный диагноз и назначили эффективное лечение.
Независимый эксперт пересматривает результаты диагностики, а также назначения лечащего врача, и выносит собственный вердикт.
Получить второе мнение особенно важно, если была назначена операция. Во многих случаях эта практика позволяет в корне изменить выбранную тактику лечения и сохранить высокое качество жизни пациента. Еще одним плюсом услуги второе мнение является возможность получить дополнительную информацию о своем заболевании и выбранной схеме лечения.
Пациенты, которым рекомендовали радикальную простатэктомию, должны задать врачу, как минимум, три вопроса:. Врачи-координаторы компании МедТур сотрудничают с большим количеством медицинских учреждений и врачей в Украине и за рубежом. Заполните онлайн-форму и они порекомендуют вам лучших независимых экспертов в области лечения рака предстательной железы.
Источники: cancer. Опубликовано: Обновлено: Выберете удобное время для разговора Введите ваш e-mail. Опишите свою ситуацию. Прикрепить выписки. Если у вас есть результаты вашего медицинского обследования, вы можете отправить их вместе с историей болезни.
Это поможет врачам разобраться в вашем вопросе. Я даю согласие на обработку моих персональных данных. Какие виды хирургии рака простаты существуют?
К преимуществам минимально инвазивной техники относятся: снижение риска инфекции и кровотечения; отсутствие заметных шрамов после операции; минимизация риска развития спаечного процесса; быстрое и менее болезненное восстановление пациента. Роботизированная простатэктомия Роботизированная или робот ассистированная простатэктомия представляет собой хирургическое вмешательство, которое проводится с помощью медицинского робота Да Винчи.
Быстрые факты о нервосберегающей роботизированной хирургии простаты: продолжительность операции — от 3 до 4 часов; особенность — возможность избежать повреждения нервных структур и связанных с этим осложнений; среднее время пребывания в стационаре — 1 день в особых случаях 2—3 дня ; преимущества — возможность сохранить эректильную функцию и избежать развития недержания мочи. Хотите узнать больше о нервосберегающей роботизированной простатэкомии? Хотите узнать больше об однопортовой простатэктомии?
Рак предстательной железы РПЖ является одним из наиболее часто встречающихся злокачественных новообразований у мужчин. В США заболеваемость РПЖ находится на одном из первых мест в структуре онкологической заболеваемости и составляет случая на тыс.
Рак предстательной железы — наиболее распространенная солидная опухоль в Европе с показателем заболеваемости случаев на мужчин, который превосходит таковые для рака легкого и колоректального рака [3]. В г. РПЖ занял 3-е место в структуре онкологических заболеваний у мужчин России, зафиксировано 29 новых случаев заболевания, пациентов умерли от РПЖ.
В связи с успехами ранней диагностики РПЖ за последние два десятилетия изменился и подход к его лечению. Общепризнанным стандартом лечения локализованного РПЖ в настоящее время является радикальная простатэктомия РПЭ [5—8].
Большое распространение РПЭ получила вследствие того, что она в наибольшей степени соответствует понятиям об «идеальной» операции применительно к лечению больных локализованными формами РПЖ: радикальность, абластичность, высокая вероятность сохранения дооперационного качества жизни, отсутствие или малая вероятность каких-либо осложнений [9].
Хирургическое лечение РПЖ в стадии T3 считалось нежелательным из-за высокого риска выявления позитивного хирургического края и метастазов в лимфатические узлы. В то же время риск смерти от РПЖ высокого риска прогрессирования снижается вдвое после радикального лечения по сравнению с наблюдением или только гормонотерапии [7, 13, 14].
При этом результаты использования РПЭ на современном этапе нельзя считать оптимальными. Одним из наиболее «фатальных» осложнений после РПЭ является рецидив заболевания [15].
Это следует принимать во внимание при рассмотрении вопроса адъювантной или спасительной лучевой терапии, гормоно-, химиотерапии или совмещения нескольких методик одномоментно [17]. Ранее исторически под рецидивом понимали опухоль, пальпируемую через прямую кишку, а также отдаленные метастазы.
В настоящее время признаком рецидивом принято считать рост уровня ПСА. Также признается важность интерпретации надира ПСА. Так, T. Uchida и соавт. В отсутствие симптомов эти исследования редко обнаруживают опухоль, так как рост уровня ПСА обычно происходит за 6—48 мес до явного рецидива. Несмотря на то что определение уровня ПСА остается наиболее чувствительным методом в диагностике рецидивов, он не позволяет дифференцировать локализованную форму от метастатической [29].
В этом важную роль играют методы визуализации [30]. Так, КТ и сцинтиграфию костей используют для выявления отдаленных метастазов в лимфатических узлах и костях, а трансректальную ультразвуковую, эндоректальную МРТ и позитронно-эмиссионную томографию ПЭТ — для диагностики местного рецидива [31, 32]. Пальцевое ректальное исследование при нулевом или очень низком уровне ПСА обычно не приносит результатов и характеризуется низкой диагностической ценностью [32]. Трансректальное УЗИ. Это исследование используют при подозрении на рецидив РПЖ после РПЭ как наиболее простой и доступный метод, хотя и рекомендуют дополнять это исследование МРТ органов малого таза [34].
Иногда эндоректальную ультрасонографию используют совместно с МРТ при местном рецидиве после РПЭ для биопсии подозрительных участков [35]. Один из новых методов обнаружения рецидивов — сцинтиграфия с антителами к простатическому мембранному антигену простасцинт. Одним из наиболее перспективных методов диагностики является МРТ, которая все чаще применяется в диагностике местных рецидивов после РПЭ [38—40]. Позитронно-эмиссионную томографию ПЭТ рекомендуют для ранней диагностики рецидивов различных опухолей.
По данным М. Picchio и соавт. На сегодняшний день «золотого» стандарта диагностики рецидива РПЖ нет, а перечисленные методы имеют ограниченные возможности в определении анатомической локализации рецидива РПЖ, особенно у пациентов с низкими значениями ПСА [29], хотя самым объективным методом выявления локального рецидива после РПЖ остается морфологическое исследование образцов, полученных в ходе трансректальной биопсии зоны везикоуретрального анастомоза [25, 45].
С учетом этих данных биопсию из зоны анастомоза обычно не берут, а ориентируются на уровень ПСА и скорость его удвоения. Кроме того, выживаемость при доказанных рецидивах примерно такая же, как при регистрации изолированного повышения ПСА. Сроки и тактика лечения при подъеме уровня ПСА после простатэктомии вызывают бурные дискуссии. В случае рецидива после операции возможны наблюдение, облучение ложа опухоли, HIFU-терапия рецидива, гормонотерапия рака простаты, а также различные сочетания гормональной, лучевой и химиотерапии [16].
Динамическое наблюдение при рецидиве рака простаты с последующей гормонотерапией. Наблюдение обычно проводят при индексе Глисона менее 7, позднем через 2 года после операции повышении уровня ПСА и времени его удвоения более 10 мес. В таких случаях медиана времени до возникновения метастазов составляет 8 лет, медиана времени от возникновения метастазов до наступления летального исхода — еще 5 лет.
Однако ее влияния на выживаемость до сих пор не установлено. При ранней гормонотерапии метастазы возникают реже, чем при отсроченной, выживаемость в обоих случаях примерно одинаковая. Необходимость гормонотерапии подтверждает исследование МRС, в котором рецидив был отмечен у всех больных, получивших лучевую терапию по поводу роста уровня ПСА после простатэктомии при опухолях рТ3b, рТхN1 и индексе Глисона 8.
Монотерапию антиандрогенными препаратами больные переносят лучше, чем комбинированную реже возникают приливы, снижение потенции, утрата полового влечения , однако антиандрогены вызывают гинекомастию и боль в сосках.
Таким образом, антиандрогены могут быть альтернативой кастрации при повышении уровня ПСА после радикального лечения особенно у относительно молодых больных без сопутствующих заболеваний. Дистанционная лучевая терапия. Если больной ослаблен или возражает против облучения, при местном рецидиве возможно динамическое наблюдение. Полученные данные подкреплены результатами других исследований [52—54], показавших существенные различия показателей 5-летней общей и безрецидивной выживаемости у больных, получавших «спасительную» лучевую терапию при выявлении только биохимического или местного рецидива в виде пальпируемых узловых образований после РПЭ.
В исследовании G. Stephenson и соавт. Исследуемая группа включила больных с биохимическим рецидивом после РПЭ, получавших лечение в 17 североамериканских центрах. Egewa и соавт. Тем не менее в связи с отсутствием результатов крупных рандомизированных исследований, а также длительного периода наблюдения влияние данного факта на показатели отдаленной выживаемости больных остается неясным [55].
Описаны случаи спасительной лучевой терапии с использованием интенсивности модулированной лучевой терапии IMRT с одновременным интегрированным повышением SIB поглощения в местном рецидиве рака простаты после РПЭ с биологической эффективностью и без серьезной острой токсичности [47]. Число таких наблюдений также ограничено. Показание к HIFU-терапии в случае рецидива в зоне пузырно-уретрального анастомоза: наличие визуализируемого участка, чья злокачественность доказана морфологически, а также исключено отдаленное метастазирование [56].
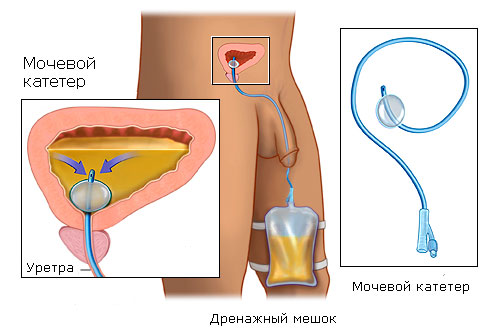
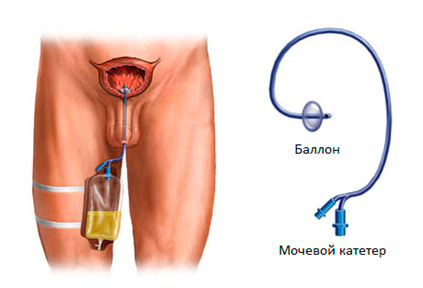
Самым крупным по числу больных является исследование M. Tasso и соавт. При этом не сообщается о каких-либо интра- и послеоперационных осложнениях. В пилотном исследовании A. Asimakopoulos и соавт. Использовался аппарат Ablatherm, процедура в среднем занимала 32 мин. Время дренирования уретральным катетером в среднем составило 7 дней. Отмечено 2 случая острой задержки мочеиспускания после удаления катетера. В данных случаях проблема была разрешена более длительным дренированием мочевого пузыря 14 и 15 дней.
Из них у 4 пациентов в первые 6 мес отмечено стрессовое недержание мочи. У 2 больных недержание разрешилось после комплекса укрепляющих упражнений, 2 пациента перенесли дополнительные малоинвазивные манипуляции для коррекции недержания.
У больных с недержанием до HIFU-терапии явления инконтиненции не усилились. Прочих осложнений не наблюдалось. Авторы считают, что HIFU-терапия местного рецидива при соответствующем отборе пациентов является эффективным мини-инвазивным методом лечения с приемлемой частотой осложнений [58].
Hayashi и соавт. Двум пациентам HIFU-терапия выполнена дважды. Сроки наблюдения варьировались от 7 до 18 мес. Осложнений выявлено не было. Murota-Kawano и соавт. При этом трое из них перед этим перенесли также спасительную дистанционную лучевую терапию. Срок наблюдения составил 6—31 мес. Осложнений, связанных с манипуляцией, не наблюдалось. Лечение локального рецидива после РПЭ высокоинтенсивным фокусированным ультразвуком относится к категории высокоэффективных методов.
Оперативное лечение. Даже с местным рецидивом РПЖ при отсутствии отдаленных метастазов и наличии вторичного поражения опухолью мочевого пузыря, вызывающего обструкцию мочеточников, гематурию и другие осложнения, негативно сказывающиеся на качестве жизни больных, эффективно выполнение радикальной цистэктомии с последующим выбором того или иного вида деривации мочи [61, 62]. В работе [63] приводятся данные по результатам проведения робот-ассистированной спасительной радикальной простатэктомии СРПЭ 34 пациентам с рецидивом РПЖ.
У 1 пациента интраоперационно была повреждена прямая кишка, что в дальнейшем потребовало наложения колостомы.
У 17 больных до операции сохранялась потенция. После робот-ассистированной СРПЭ число больных с эректильной функцией сократилось до 7. У троих больных развилась рубцовая деформация в зоне анастомоза, корригированная эндоскопическим путем.
Криотерапия при рецидиве после РПЭ. Cпасительная криотерапия остается разумным выбором для лечения местного рецидива РПЖ при соответствующем отборе пациентов [64].
Имеется опыт использования брахитерапии в качестве основной процедуры спасательного средства для лечения местного рецидива после РПЭ со средней дозой, которая составила Гр [34]. Подтверждена целесообразность и безопасность спасительной брахитерапии в качестве возможного альтернативного варианта дистанционной лучевой терапии для лечения местного рецидива РПЖ у отдельных больных [66].
Позитронно-эмиссионная томография пока не получила широкого распространения, во многом и из-за низкой доступности для пациентов, однако, вероятно, является весьма перспективным методом и будет в дальнейшем активно внедряться в практическую медицину.
В остальных случаях предпочтительно наблюдение с последующей гормонотерапией.
Также при местном рецидиве после РПЭ возможно выполнение оперативного лечения, HIFU-терапии, крио- и брахитерпии, а также использование иных малоинвазивных методик. Сравнивать эти методики пока рано, так как период наблюдения после «спасительных» аблативных методов лечения в мире небольшой.
Chissov V. National leadership. Russian Чиссов В. Национальное руководство. Chang S. Prostate-specific membrane antigen: Present and future applications. Boyle P. Cancer incidence and mortality in Europe Ann Oncol. Kaprin A. The state of cancer care the population of Russia in Russian Каприн А. Состояние онкологической помощи населению России в году. Vеliyev E. Improving recidivism survival after radical prostatectomy for locally advanced prostate cancer, depending on the duration of surgery.
Russian Велиев Е. Улучшение рецидивной выживаемости после радикальной простатэктомии при местно-распространенном раке предстательной железы в зависимости от срока оперативного вмешательства.
Pushkar D. Radical prostatectomy. Russian Пушкарь Д. Радикальная простатэктомия. Abdollah F. Survival benefit of radical prostatectomy in patients with localized prostate cancer: estimations of the number needed to treat according to tumor and patient characteristics.
Augustin H. Intraoperative and perioperative morbidity of contemporary radical retropubic prostatectomy in a consecutive series of patients: results of a single center between and Petrov S. Surgical treatment of localized forms of prostate cancer. Russian Петров С. Хирургическое лечение локализованных форм рака предстательной железы.
Isbarn H. Long-term data on the survival of patients with prostate cancer treated with radical prostatectomy in the prostate-specific antigen era. BJU Int. Porter C.
Peeters S. Dose-response in radiotherapy for localized prostate cancer: results of the Dutch multicenter randomized phase III trial comparing 68 Gy of radiotherapy with 78 Gy. J Clin Oncol. Warde P. Combined androgen deprivation therapy and radiation therapy for locally advanced prostate cancer: a randomised, phase 3 trial.
Wilt T. Pereverzev A. Prostate cancer. Kharkov: Fact. Russian Переверзев A. Рак простаты. Харьков: Факт. Solovov V.